隨后的細胞實驗發現 , 敲除hnRNP K , 能減弱肝癌細胞增殖和遷移侵襲的能力 , 并且還能消除lnc-CTHCC過表達對肝癌細胞增殖和轉移的促進作用;而過表達hnRNP K , 則能挽救lnc-CTHCC敲除導致的肝癌細胞增殖和遷移能力的下降 。 另外 , hnRNP K還能調節腫瘤轉移相關標志物的表達 。 由此可見 ,lnc-CTHCC通過直接結合hnRNP K參與肝癌的發生和轉移 。

文章圖片
▲ 免疫沉淀顯示lnc-CTHCC和hnRNP K結合( 圖d);hnRNP K在肝癌組織中表達升高( 圖i);hnRNP K高表達與肝癌患者的預后降低顯著相關( 圖m);敲除hnRNP K后 , 肝癌細胞增殖(圖n和圖o)和遷移侵襲(圖p)的能力減弱;hnRNP K過表達挽救了lnc-CTHCC敲除對肝癌細胞增殖和轉移的抑制作用 (圖q);hnRNP K敲除抵消了lnc-CTHCC過表達對肝癌細胞增殖和轉移的促進作用( 圖r)
為了進一步確定lnc-CTHCC在hnRNP K后的下游機制 , 研究人員檢測了lnc-CTHCC在肝癌中調控的信號通路 , 發現與細胞生長相關的Hippo信號通路 , 在lnc-CTHCC敲除的肝癌組織中明顯富集 , 其中 , 通路的核心蛋白YAP1水平顯著降低 。
染色質免疫沉淀發現hnRNP K與YAP1啟動子區域結合 , 熒光素酶報告基因實驗證明敲除hnRNP K能降低YAP1的轉錄活性 。 這些結果表明 ,在與hnRNP K直接結合后 , lnc-CTHCC募集hnRNP K至YAP1啟動子區域 , 促進YAP1轉錄 。
YAP1作為一種癌基因 , 在多種癌癥中表達上調 , 能促進癌癥細胞的增殖和存活[6] 。 那么 , lnc-CTHCC是否是通過YAP1來促進肝癌的發生呢?
為了確定YAP1在肝癌中的生物學功能 , 研究人員驗證了YAP1在肝癌中的表達水平:YAP1在肝癌組織中高表達 , 高YAP1與總生存率降低顯著相關 。 敲除YAP1 , 肝癌細胞增殖和遷移侵襲能力減弱 , 并且能消除lnc-CTHCC過表達對肝癌細胞增殖和轉移的增強效應 。 在小鼠肝癌模型中 , YAP1基因敲除能顯著抑制lnc-CTHCC誘導的腫瘤生長 。 這些結果表明 ,lnc-CTHCC依賴于YAP1促進肝癌細胞的惡性表型 。
文章圖片
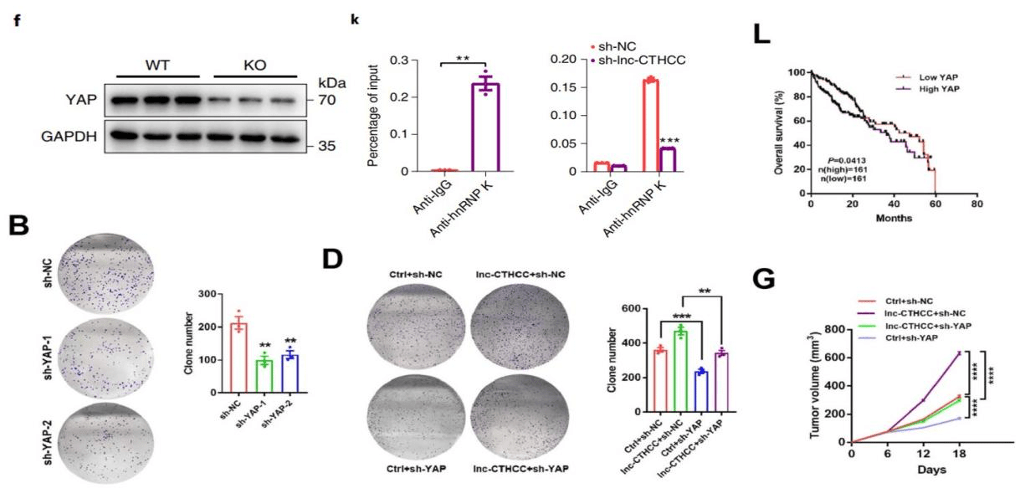
▲ lnc-CTHCC敲除后 , YAP1表達降低( 圖f);hnRNP K與YAP1啟動子區域結合( 圖k);高YAP1與肝癌總生存率降低顯著相關( 圖L);敲除YAP1 , 肝癌細胞增殖減弱(圖B) , 并且能消除lnc-CTHCC過表達對肝癌細胞增殖的促進效應(圖D);在肝癌小鼠中 , 敲除YAP1抑制lnc-CTHCC誘導的腫瘤生長( 圖G) 。
【癌癥|《自然·癌癥》:南京鼓樓醫院團隊發現肝癌發病新機制】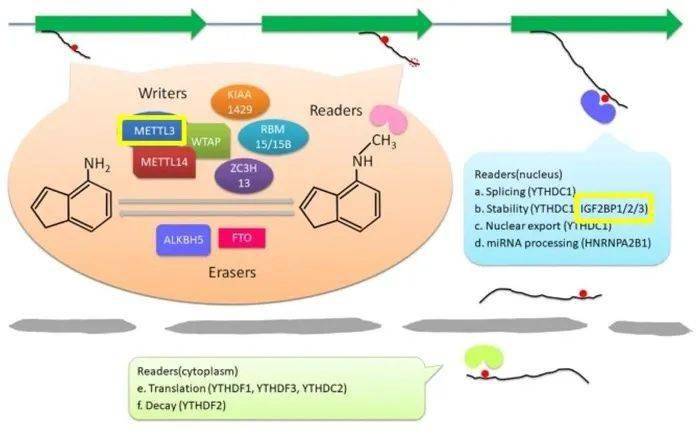
文章圖片
▲ m6A修飾的功能(黃框所示為本文涉及的三個相關蛋白)
研究人員發現 , 作為一種lncRNA , 在肝癌中 ,lnc-CTHCC的m6A修飾水平顯著上升 。 敲除或過表達METTL3 , 能相應地下調或上調lnc-CTHCC表達 , 進而抑制或促進肝癌細胞的惡行生物學行為 。 因此 , METTL3通過增加對lnc-CTHCC的m6A修飾 , 上調lnc-CTHCC的表達 , 發揮對肝癌細胞的調節功能 。
文章圖片
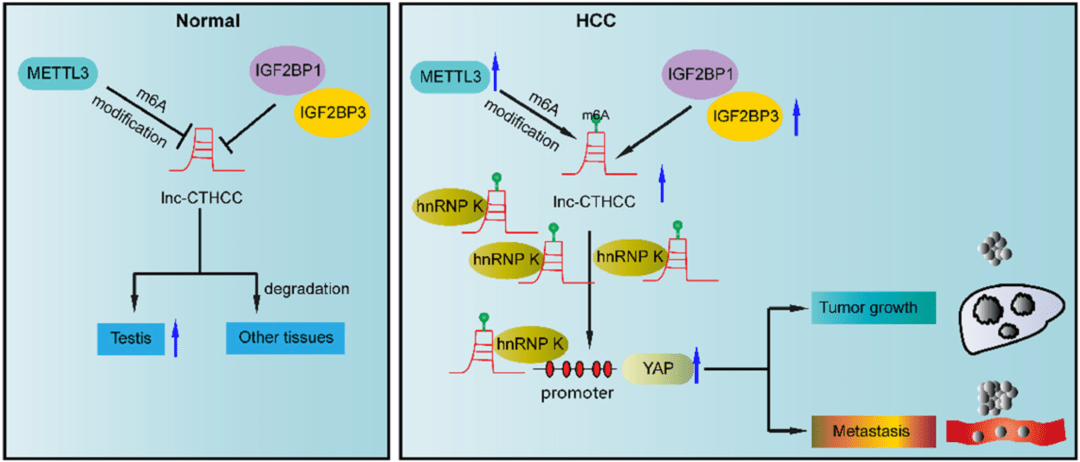
▲ 本文機制示意圖(Normal:正常組織;HCC:肝癌組織)
本研究中 , 研究人員先是通過生信分析 , 發掘和鑒定了一個新的CT基因 , lnc-CTHCC;爾后 , 通過一系列的實驗 , 探索和驗證了lnc-CTHCC在METTL3–IGF2BP1/IGF2BP3–lnc-CTHCC–hnRNP K–YAP1軸中發揮的關鍵作用 。 整個過程絲絲入扣 ,創新性地提出CT-lncRNA是驅動肝癌發生的新靶標 , 有望為肝癌的個性化治療提供新思路 。
- 楊女士|癌癥治與不治都是死,不如花錢游山玩水腫瘤科主任說出了大實話
- 胰腺癌|癌癥來臨時,身體會“喊痛”!身上若出現5種痛,千萬別大意了
- 從容|《2022安盛心理健康狀況調研報告》:新冠疫情挑戰為心理健康發展帶來契機,健康意識和韌性均顯著提升
- 綠茶|我們怕癌,但是癌更害怕它們,盡量多吃這3種食物,讓癌癥遠離你
- 研究人員|喝茶不養生,還可能“養癌”?50萬國人研究:喝茶與多種癌癥有關
- 傾向|家族當中有幾個近親得了癌癥,我們應該怎么做?
- 飲食|想要預防癌癥,要在飲食上做出一定改變,提醒:3樣食物盡量少吃
- 因素|焦慮男易患兩大疾病
- 有“癌癥抗體”的人,可能有這6個“共性”,你有嗎?
- 癌癥|孩子出現關節痛、瘀斑等癥狀,家長需警惕這種疾病
