肝癌是最常見、也是最致命的消化道惡性腫瘤之一 。
然而 , 發病機制的不清 , 使得肝癌的治療手段局限[1] 。 因此 , 迫切需要尋找肝癌發生發展過程中新的驅動分子 , 以研發更加有效的治療方法 , 提高肝癌患者的預后 。
癌癥—睪丸基因(CT基因)是原本僅僅在睪丸中特異表達的基因 , 但在腫瘤發生過程中被重新激活 , 也在腫瘤組織中高表達 , 驅動腫瘤的惡性進程[2] 。 腫瘤發生與精子發生的相似性 , 使得CT基因成為癌癥潛在的驅動基因和富有希望的治療靶點 。
近日 ,南京鼓樓醫院肝膽胰中心孫倍成教授 , 聯合南京醫科大學生殖醫學國家重點實驗室胡志斌教授和南京大學醫學院王守宇教授 , 發現一種新的CT基因 , 命名為 lnc-CTHCC , 并證實它在METTL3–IGF2BP1/IGF2BP3–lnc-CTHCC–hnRNP K–YAP1軸中發揮關鍵作用 , 導致肝癌的發生和發展[3] 。 研究成果在線發表在最新一期的著名醫學期刊《自然·癌癥》 。

文章圖片
▲ 論文首頁截圖
首先 , 研究人員聯合GTEx和TCGA數據庫 , 從中發掘出一個新的基因 , 在睪丸中特異表達 , 同時也在腫瘤中高表達 。 經鑒定 , 它 符合CT基因的表達模式 , 同時也是一種lncRNA , 于是將其命名為lnc-CTHCC 。
接著 , 研究人員對lnc-CTHCC進行了檢測 , 發現 lnc-CTHCC在肝癌的細胞株和臨床樣本中表達明顯升高 , 且與肝癌體積、AFP水平、癌癥分期和血管侵犯顯著相關 , 還是影響肝癌患者預后的獨立危險因素 。
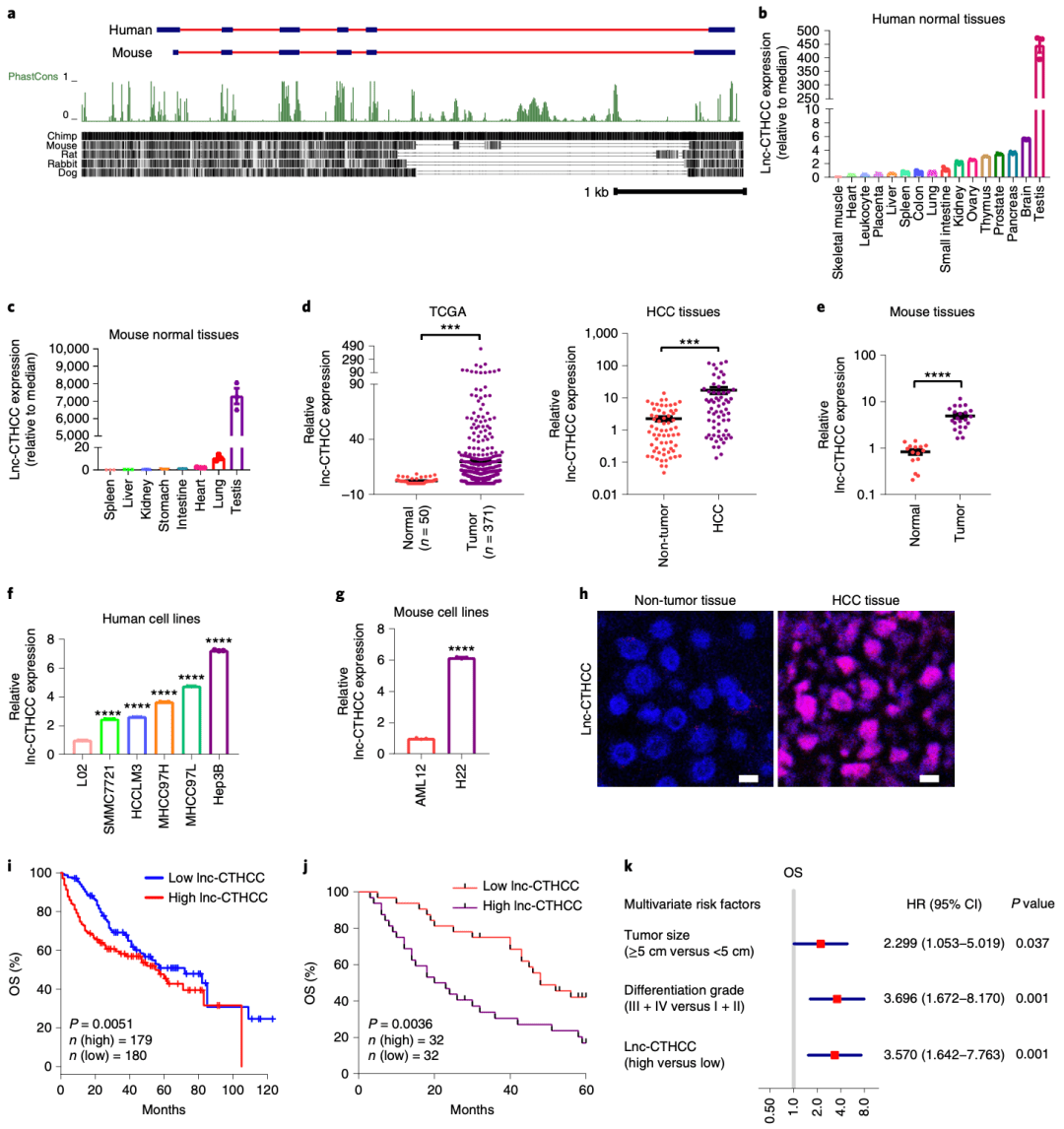
文章圖片
▲ 正常情況下lnc-CTHCC只在睪丸中特異表達( 圖b);lnc-CTHCC在肝癌細胞株(圖f)和肝癌組織(圖d)中高表達(HCC為肝癌 , L02為正常肝細胞株 , 其余5種為肝癌細胞株);lnc-CTHCC高表達和肝癌預后差(圖j)以及臨床病理特征(圖k)相關 。
隨后 , 研究人員進行了表型實驗 , 探究lnc-CTHCC在肝癌發生中的作用 。
敲除lnc-CTHCC后 , 肝癌細胞的增殖、遷移和侵襲能力減弱 , 腫瘤血管生成減少;而過表達lnc-CTHCC , 則加快肝癌類器官生長速度 , 上調促血管生成因子的表達 。 細胞實驗表明 ,lnc-CTHCC能促進肝癌的增殖、轉移和血管生成 。
研究人員又構建了lnc-CTHCC基因敲除小鼠 , 然后誘導肝癌形成 。 結果發現 , 敲除lnc-CTHCC后 , 肝癌小鼠的瘤體質量和數量減小 , 肝臟炎癥水平和纖維化程度下降 , 微血管密度降低 , 細胞增殖減弱和凋亡增多 , 肝癌肺轉移被抑制 。 動物實驗表明 ,lnc-CTHCC缺失能抑制肝癌的發生和發展 。
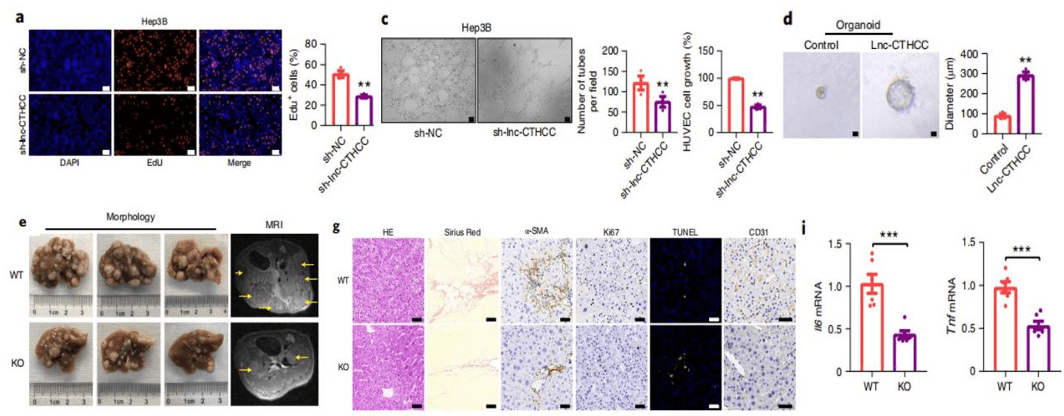
文章圖片
▲ 敲除lnc-CTHCC后 , 肝癌細胞增殖減慢(圖a) , 腫瘤血管生成減慢(圖c);過表達lnc-CTHCC后 , 肝癌類器官生長加快;lnc-CTHCC敲除后 , 肝癌小鼠瘤體質量和數量減小(圖e) , 肝臟炎癥水平(圖i)下降 , 微血管密度降低 , 細胞增殖減弱和凋亡增多(圖g) 。
表型實驗的成功讓研究人員對lnc-CTHCC促進肝癌的分子機制進行了探究 。
考慮到ncRNA通常通過結合特定的蛋白質發揮功能[4] , 研究人員獲得了與lnc-CTHCC直接結合的蛋白質 , 他們把目光鎖定在了 hnRNP K上 。
hnRNP K屬于RNA結合蛋白 , 也是一種轉錄因子 , 既往研究發現其表達的異常與多種腫瘤的發生密切相關[5] 。 于是 , 研究人員也在肝癌組織中進行了檢測 , 發現 hnRNP K表達升高 , 而且與肝癌患者的預后差顯著相關 。
- 楊女士|癌癥治與不治都是死,不如花錢游山玩水腫瘤科主任說出了大實話
- 胰腺癌|癌癥來臨時,身體會“喊痛”!身上若出現5種痛,千萬別大意了
- 從容|《2022安盛心理健康狀況調研報告》:新冠疫情挑戰為心理健康發展帶來契機,健康意識和韌性均顯著提升
- 綠茶|我們怕癌,但是癌更害怕它們,盡量多吃這3種食物,讓癌癥遠離你
- 研究人員|喝茶不養生,還可能“養癌”?50萬國人研究:喝茶與多種癌癥有關
- 傾向|家族當中有幾個近親得了癌癥,我們應該怎么做?
- 飲食|想要預防癌癥,要在飲食上做出一定改變,提醒:3樣食物盡量少吃
- 因素|焦慮男易患兩大疾病
- 有“癌癥抗體”的人,可能有這6個“共性”,你有嗎?
- 癌癥|孩子出現關節痛、瘀斑等癥狀,家長需警惕這種疾病
