團隊|武漢大學(xué)李紅良教授團隊在心血管代謝性疾病領(lǐng)域連續(xù)取得重要進展
央廣網(wǎng)北京2月23日消息 當前 , 心血管代謝性疾病已經(jīng)成為威脅人類健康的第一殺手 , 據(jù)統(tǒng)計 , 我國心血管疾病患者高達3.3億人、代謝性疾病患者約4.5億人 , 其發(fā)病率仍持續(xù)上升 , 成為嚴重威脅人民健康的重大公共衛(wèi)生問題 。 有效防治此類疾病的關(guān)鍵是全面而深入認識和解析其病理生理學(xué)及分子生物學(xué)機制 , 并在此基礎(chǔ)上開發(fā)相關(guān)藥物等防治和診療策略 。
武漢大學(xué)李紅良團隊始終聚焦于心血管及代謝性疾病領(lǐng)域的重大問題 , 探索該領(lǐng)域重大疾病的重要分子生物學(xué)機制 , 并開展轉(zhuǎn)化研究、藥物開發(fā)和臨床研究 。 該團隊近年來在該領(lǐng)域 , 特別是在非酒精性脂肪肝病(NAFLD)及其相關(guān)疾病研究領(lǐng)域不斷取得重大突破和重要成果 , 累計在Nature Medicine、Cell Metabolism、Circulation、Science Translational Medicine、Journal of Hepatology、Circulation Research、Hepatology 等一流期刊發(fā)表研究論文200多篇 。
【團隊|武漢大學(xué)李紅良教授團隊在心血管代謝性疾病領(lǐng)域連續(xù)取得重要進展】2021年 , 我們關(guān)注到李紅良團隊共發(fā)表29項重要的研究成果 , 其中SCI影響因子高于10的有15篇 , 高于20的有5篇 。 2021年 , 李紅良團隊研究領(lǐng)域涵蓋了心血管疾病、代謝性疾病和新冠肺炎臨床大數(shù)據(jù)研究等領(lǐng)域 , 闡明了一系列心臟疾病、脂肪肝炎、缺血再灌注損傷等臨床重大疾病的重要發(fā)病機制 , 發(fā)現(xiàn)了一批關(guān)鍵作用靶點 , 研發(fā)出一系列小分子先導(dǎo)藥物 。 為認識心血管代謝性疾病提供了新的重要理論基礎(chǔ) , 也為該領(lǐng)域新藥開發(fā)提供了一系列新的思路及潛在靶點 。
iNature按照領(lǐng)域系統(tǒng)總結(jié)了其中的主要研究成果:
研發(fā)全新心血管代謝性疾病創(chuàng)新治療藥物
心血管代謝性疾病已成為導(dǎo)致人類死亡的頭號殺手 。 為了解決心血管代謝性疾病的發(fā)病機制和臨床治療問題 , 李紅良教授團隊近十多年來綜合運用生物大數(shù)據(jù)、疾病動物模型、人工智能藥物設(shè)計等前沿技術(shù) , 發(fā)現(xiàn)花生四烯酸通路是心臟、肝臟缺血再灌注損傷和脂肪肝炎的核心發(fā)病機制 , 并進一步找到了最關(guān)鍵的治療靶點—12-脂氧合酶(ALOX12) 。 根據(jù)這一重要靶點 , 研究團隊開發(fā)出了3種高效安全的先導(dǎo)化合物 , 其中一種全新的小分子化合物(IMA-1)可精準靶向ALOX12-ACC1蛋白相互作用 , 顯著抑制小鼠和食蟹猴脂肪肝炎發(fā)生發(fā)展 。 更為重要的是 , 這一新開發(fā)的先導(dǎo)化合物不會引起高血脂等副作用 。 系列研究突破性解決了靶向ACC的副作用問題 , 破解了靶向ACC治療脂肪肝炎的困境 。 系列成果于2021年12月15日作為封面文章在《科學(xué)·轉(zhuǎn)化醫(yī)學(xué)》雜志背靠背同時發(fā)表 , 并被列為亮點研究寫入12月17日出版的《科學(xué)》雜志特刊 。 同時 , 科研團隊還首次發(fā)現(xiàn)ALOX12小分子抑制劑ML355可有效改善小鼠、巴馬豬和恒河猴的心臟缺血再灌注損傷 , 顯著提升心功能 , 為深入探索心臟缺血再灌注損傷、改善心梗患者預(yù)后、提高患者生存率提供了重要支撐 。
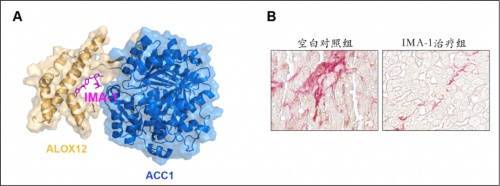
文章圖片
圖A. IMA-1抑制ALOX12和ACC1蛋白互作結(jié)構(gòu)圖;圖B. IMA-1治療脂肪肝炎效果(紅色染色區(qū)域代表肝臟纖維化程度)(企業(yè)供圖 央廣網(wǎng)發(fā))
發(fā)現(xiàn)系列代謝性疾病重要機制和關(guān)鍵靶點
肥胖、2 型糖尿病以及 NAFLD 是代謝綜合征的主要誘因 , 為了更好地解決這些健康威脅 , 李紅良教授團隊對疾病發(fā)病機制進行了深入探索 。 采用大規(guī)模系統(tǒng)生物學(xué)篩選分析、免疫熒光、過表達腺病毒處理等先進技術(shù) , 研究團隊發(fā)現(xiàn)TMBIM1是通過降低PPARγ的穩(wěn)定性而抑制脂肪生成 , 是一種有效抑制脂肪生成的全新因子 , 為加深脂肪生成調(diào)控機制的認識提供了潛在分子靶點與新思路;發(fā)現(xiàn)Nemo樣激酶(NLK)作為一種新型肝糖異生負調(diào)控因子 , 促進CRTC2和FOXO1核輸出 , 在糖異生調(diào)節(jié)網(wǎng)絡(luò)中起著關(guān)鍵作用 , NLK可能成為2型糖尿病的潛在治療靶點;為了進一步闡明NAFLD的發(fā)病機制 , 研究團隊還發(fā)現(xiàn)了一系列重要分子 , 如MAVS、SNX8、RNF5、RGS5等 , 它們都是NAFLD發(fā)展的關(guān)鍵分子 , 是NAFLD預(yù)防和治療的潛在藥物靶點 。 系列研究成果發(fā)表在Cell Metabolism、Hepatology等國際權(quán)威雜志 。
- 疫情|武漢通報9例新增核酸檢測陽性感染者相關(guān)情況及活動場所
- 團隊|【都勻這家醫(yī)院牛!】一周完成三例高難度手術(shù),貴州首例在其中!
- 網(wǎng)站|湖北2月22日新增新冠肺炎本土確診病例5例 均在武漢市
- 人員|“如新公司”武漢培訓(xùn)致多人感染 涉事酒店同期有180多人入住 如新總部:經(jīng)銷商私辦年會
- 車站街道|武漢市新冠肺炎疫情防控指揮部通告(2022年第1號)
- 轉(zhuǎn)播|河北大學(xué)附屬醫(yī)院醫(yī)療保障團隊繼續(xù)保持兩個場館醫(yī)療站全天候運轉(zhuǎn)
- 上海兒童醫(yī)學(xué)中心張海波教授團隊以“疑難復(fù)雜先天性心臟病關(guān)鍵診療技術(shù)”獲中華醫(yī)學(xué)科技獎
- 定點醫(yī)院|武漢累計確診和感染者均與某培訓(xùn)班有關(guān)
- 病例|10多人陽性,武漢這場培訓(xùn)誰組織的?
- 新聞|一目了然
