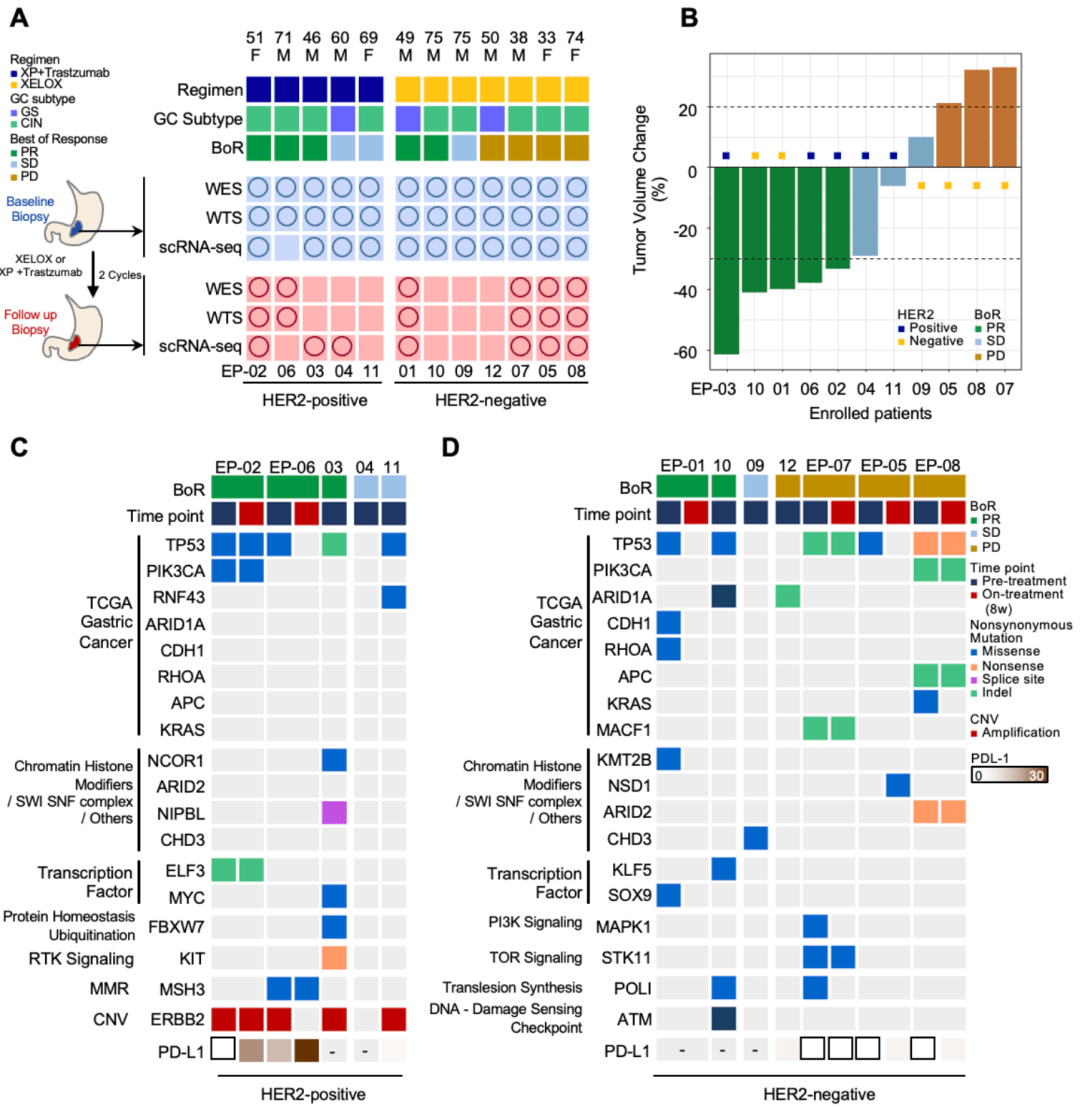
通過進一步分析兩組腫瘤的突變特征 , 研究人員發現兩組大多數的單核苷酸替換均為C:G>T:A轉換 。 WES及WTS測序的結果表明 , AGC患者在經歷2個周期化療后 , 腫瘤的基因組變化尚不顯著 , 表明它們不是影響腫瘤免疫微環境的主要因素 。
文章圖片
圖1:研究入組流程及入組患者的基因組特征
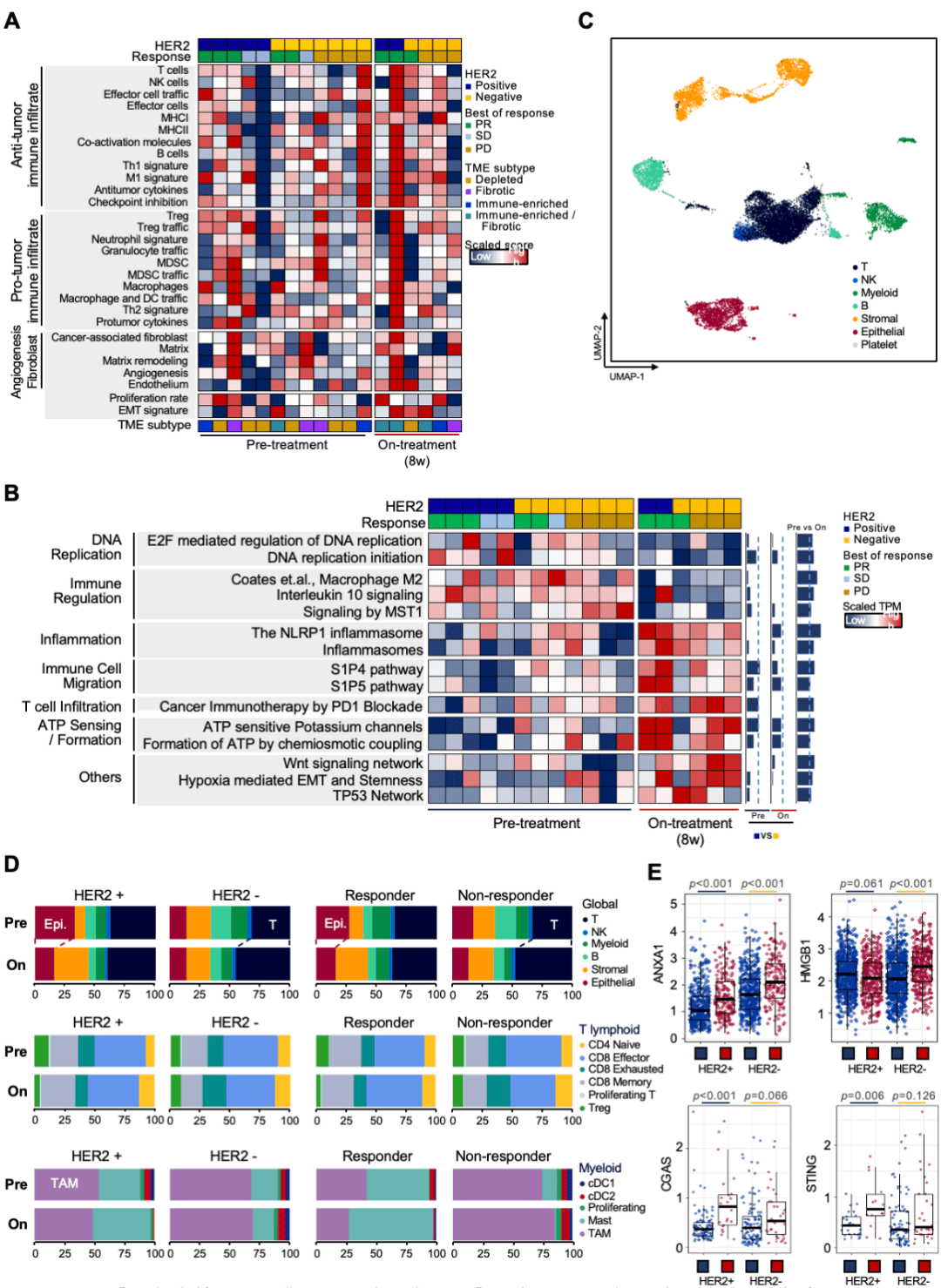
接下來 , 研究人員對化療前后的RNA-seq數據進行分析 , 并將腫瘤組織的免疫亞型分為四類:免疫缺失型、纖維化型、免疫富集型及免疫富集/纖維化型 。 所有腫瘤患者化療前的TME組成并無明顯差異 , 而 在經歷2個周期化療后 , 基因組變異分析(GSVA)發現與M2型巨噬細胞(主要發揮抗炎、免疫抑制作用)分化相關的基因顯著受抑制(P=0.009);此外 , PD-1通路相關的基因被明顯激活(P=0.033) , 尤其是在響應型患者中(圖2A-B) 。
研究人員進一步分析了治療前(n=11)及治療后(n=7)腫瘤組織的scRNA-seq結果 , 并鑒定出7種主要的細胞亞群:上皮細胞 , 間質細胞 , T細胞 , 自然殺傷(NK)細胞 , 髓樣細胞 , B細胞 , 血小板及未分類細胞 。他們發現T細胞比例在化療后的腫瘤中有增加趨勢 , 對于響應型患者而言 , 效應CD8 T細胞在化療后的中位百分比(46.1%)也明顯高于化療前(39.5%) 。 另一方面 , 在無響應型患者中 , 化療后耗竭T細胞的中位百分比(14%)也高于化療前(10.5%) 。 相比于響應型患者 , 無響應型患者中腫瘤相關巨噬細胞(TAM)的中位比例明顯升高(79.1%) , 而在化療后又進一步升高(86.7%)(圖2C-D) 。
為了明確化療對腫瘤微環境中T細胞的調控機制 , 他們對化療前后的上皮細胞中免疫信號通路的變化進行分析 。 結果發現 化療后損傷相關分子模式家族(DAMPs)的代表性基因(如ANXA1、HMGB1)的表達均顯著上調;此外 , 對于HER2陽性的患者而言 , 固有免疫信號通路中的相關基因(如cGAS、STING)的表達在化療后也明顯上調(圖2E) 。 這些結果提示 ,傳統化療藥物可能通過重組T細胞組分 , 及激活固有免疫細胞而重塑部分AGC患者的腫瘤免疫微環境 。
文章圖片
圖2:化療前后腫瘤組織信號通路及免疫微環境的變化情況
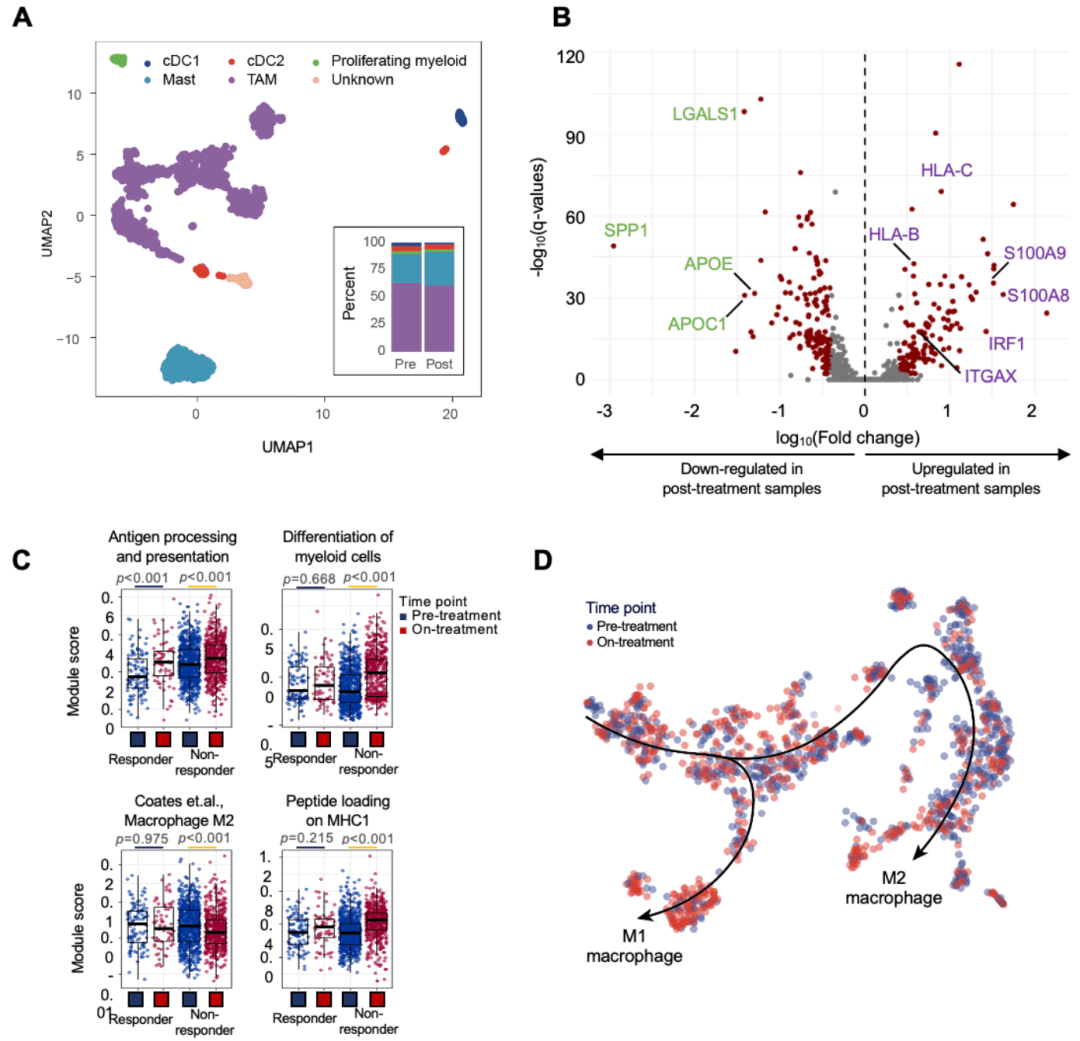
那么 , 抗原提呈細胞是否也參與免疫重塑的過程呢?為回答這個問題 , 他們將髓樣細胞細分為5個亞型 , 并重點關注腫瘤相關巨噬細胞(TAM)這一亞型 , 結果顯示在 化療前后該亞型細胞的差異表達基因高達1003個 。 其中促炎相關基因及MHC I類抗原遞呈基因在化療后顯著上調;而抗炎分子在化療后則明顯下調(圖3A-B) 。 除觀察到基因的差異表達外 , 信號通路的變化趨勢也與之類似(圖3C) 。
隨后 , 研究者還對TAM的分化軌跡進行了重建 , 將表達單細胞樣巨噬細胞分子標志物(CD14 , FCN1)的細胞群作為分化起點 , 根據擬時序分析得到兩種分化軌跡 , 一種為M2型巨噬細胞 , 另一種為M1型巨噬細胞 。 化療前腫瘤組織中 , M2型巨噬細胞的比例(91.9%)顯著高于M1型巨噬細胞(8.1%);而 經歷2個周期化療后 , M1型巨噬細胞比例顯著增加(35.8%) 。 這一數據提示化療藥物也誘導了M1/M2的極化過程 。
文章圖片
圖3:化療對TAM分化的影響
為了驗證化療藥物對TME的調控過程 , 研究人員又選擇了另一個包含17名AGC患者的臨床隊列進行驗證 , 所得結果也與前期研究結果相類似 。
- 消保委|祛斑效果不明顯消保委協調退款
- 早上起床|長壽的人,晨起后通常會有4個“共性”,堅持下去,許會有好效果
- 蛋白尿|替米沙坦好不好?優缺點都在這,服藥時注意3點,效果會更好
- 冬季如何對抗感冒 四藥膳對癥治療效果佳
- 食道瘤|成都中醫腫瘤醫院,成都中醫腫瘤研究院:食道瘤難治?看中醫專利組方如何治療!
- 抗原|腫瘤標志物,有哪些與腸癌相關?它常常“不靠譜”,為什么要用?
- 福利|助力患者全家健康 藥康付梳理出即將在中國上市的10款抗腫瘤藥物
- 胃癌|25歲小伙確診胃癌,化療離世,醫生嘆息:1菜比10斤酒還傷胃,趁早遠離
- 血糖|踩進控制血糖的3個誤區,不僅讓你白白受罪,還達不到降糖效果
- 惡性腫瘤|“小腫塊”已切除,醫生為何還“緊追不放”?仔細檢查結果讓人吃驚
