轉移是腫瘤患者死亡的主要原因之一[1] 。 不同的腫瘤轉移偏好并不相同 ,40-75%的IV期黑色素瘤患者會發生腦轉移[2,3] 。
盡管已有臨床試驗結果表明 , 黑色素瘤腦轉移灶對已經獲批的靶向療法以及免疫治療仍有響應 , 但是這種應答持續時間較短 , 大多數患者最終死于腦轉移瘤 [4-7] 。 因此 , 我們迫切需要了解黑色素瘤腦轉移機制 , 并為腦轉移的患者提供新的治療策略 。
近日 , 由 紐約大學朗格尼醫學中心的Eva Hernando教授領銜的研究團隊在 Canecr Discovery 期刊發表研究成果 [8] 。
他們發現 進入大腦的黑色素瘤細胞為了生存 , 竟然會分泌β-淀粉樣蛋白(Aβ) , 這些Aβ蛋白會招募并促進星形膠質細胞向促癌表型轉化 , 同時還能阻止小膠質細胞吞噬黑色素瘤細胞 。
讓導致阿爾茨海默病的“頭號嫌疑犯”為自己的轉移服務 , 黑色素瘤這招真是絕了!
不過 , 黑色素瘤細胞可能沒想到 , 已經用于臨床研究的Aβ抑制劑就在前面等它呢! Hernando團隊發現抑制Aβ蛋白分泌的BACE抑制劑可以減少黑色素瘤的腦轉移 。
這就是“魔高一尺道高一丈” 。

文章圖片
▲ 論文首頁截圖
為了尋找腦轉移灶腫瘤的特征 , Hernando團隊將同一個黑色素瘤患者的腦轉移灶(BM)和非腦轉移灶(NBM)中的腫瘤細胞分離出來 , 短期培養后使用短期培養物(STC)進行小鼠荷瘤實驗 , 以及無偏差蛋白質組分析 。 小鼠荷瘤實驗顯示 ,腦轉移灶來源的腫瘤細胞表現出更強的腦轉移能力 。 這表明腦轉移灶的細胞具有獨特的能力 , 能夠更好的適應大腦內的環境 。
蛋白質組分析顯示 ,腦轉移灶腫瘤細胞富集與神經退行性疾病(阿爾茨海默病、帕金森病和亨廷頓病)的蛋白質 。
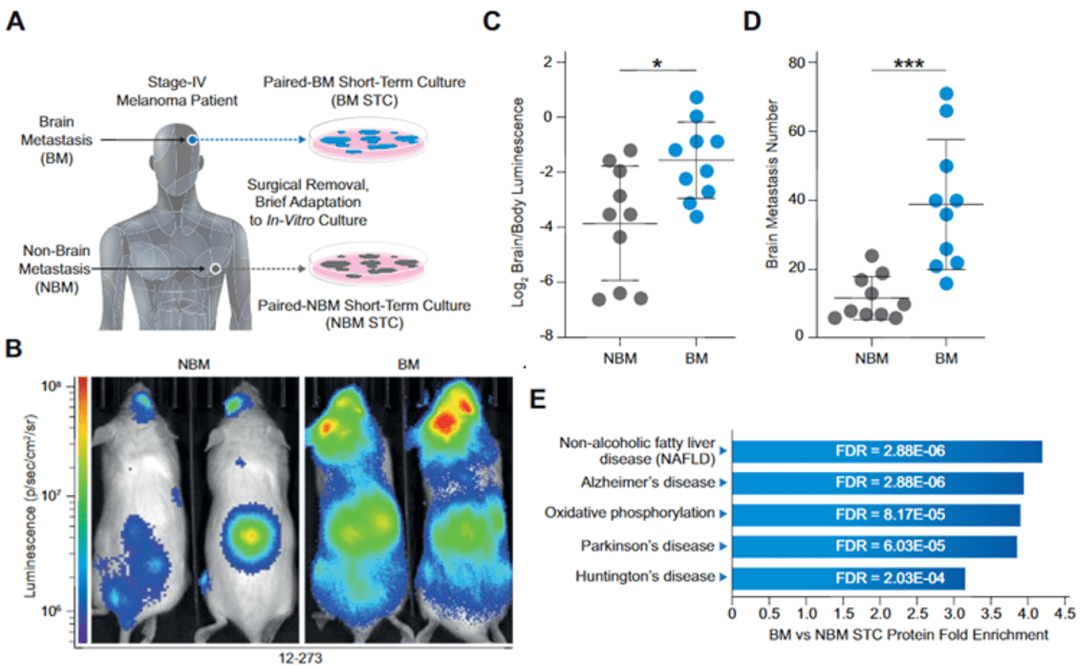
文章圖片
▲ A:標本獲取示意圖;B-D:BM-SCT具有更強的腦轉移能力;E:BM-SCT上調多種與神經退行性疾病相關通路
Hernando團隊對差異表達蛋白質的進一步調研發現 ,腦轉移灶腫瘤細胞高表達多種切割淀粉樣前體蛋白(APP)的酶 , 如α-分泌酶(BACE2)和α-分泌酶復合物的催化亞基(PSEN1);而與 減少Aβ產生相關的酶則顯著降低 , 如泛素連接酶UCHL1和ADAM19 。
那么黑色素瘤細胞是否能夠分泌Aβ呢?Hernando團隊檢測了黑色素瘤細胞培養物上清中Aβ的含量 , 結果顯示 腦轉移灶的短期培養物上清中有更多的Aβ 。 鑒于Aβ可以對大腦產生影響 , 他們假設黑色素瘤細胞可能需要Aβ來幫助它們在大腦實質中存活和生長 。
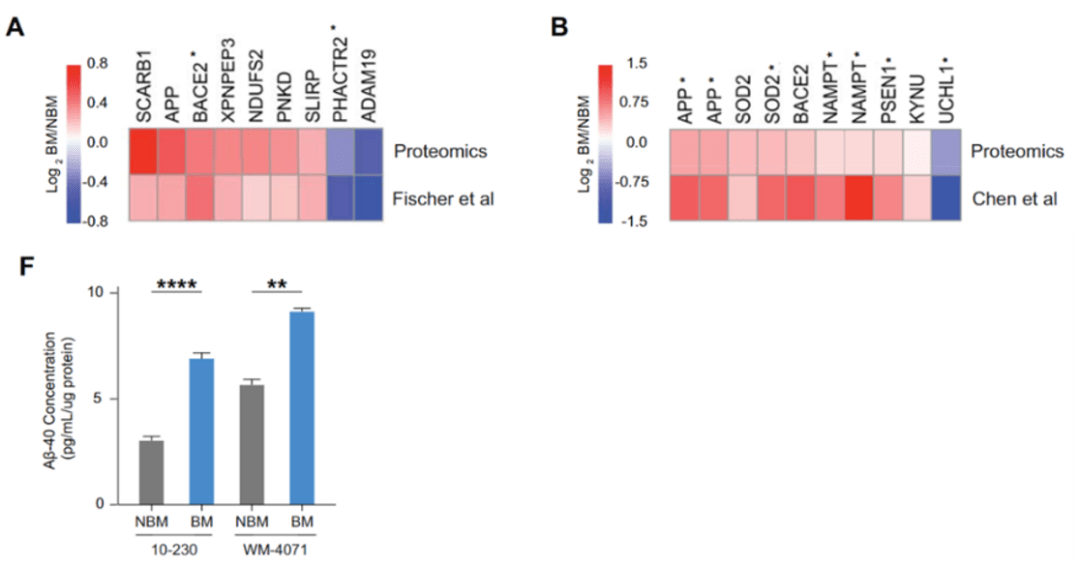
文章圖片
▲ A , B:腦轉移黑色素瘤細胞高表達切割APP的酶;F:腦轉移黑色素瘤細胞分泌更高水平的Aβ
那么Aβ是否真的能影響黑色素瘤細胞的腦轉移能力呢?Hernando團隊敲低了黑色素瘤細胞中的APP , 發現 敲低APP的黑色素瘤細胞腦轉移能力下降 , 但是顱外轉移能力沒有受到影響 。 這些結果提示 , APP是黑色素瘤細胞在大腦定植所必需的 。
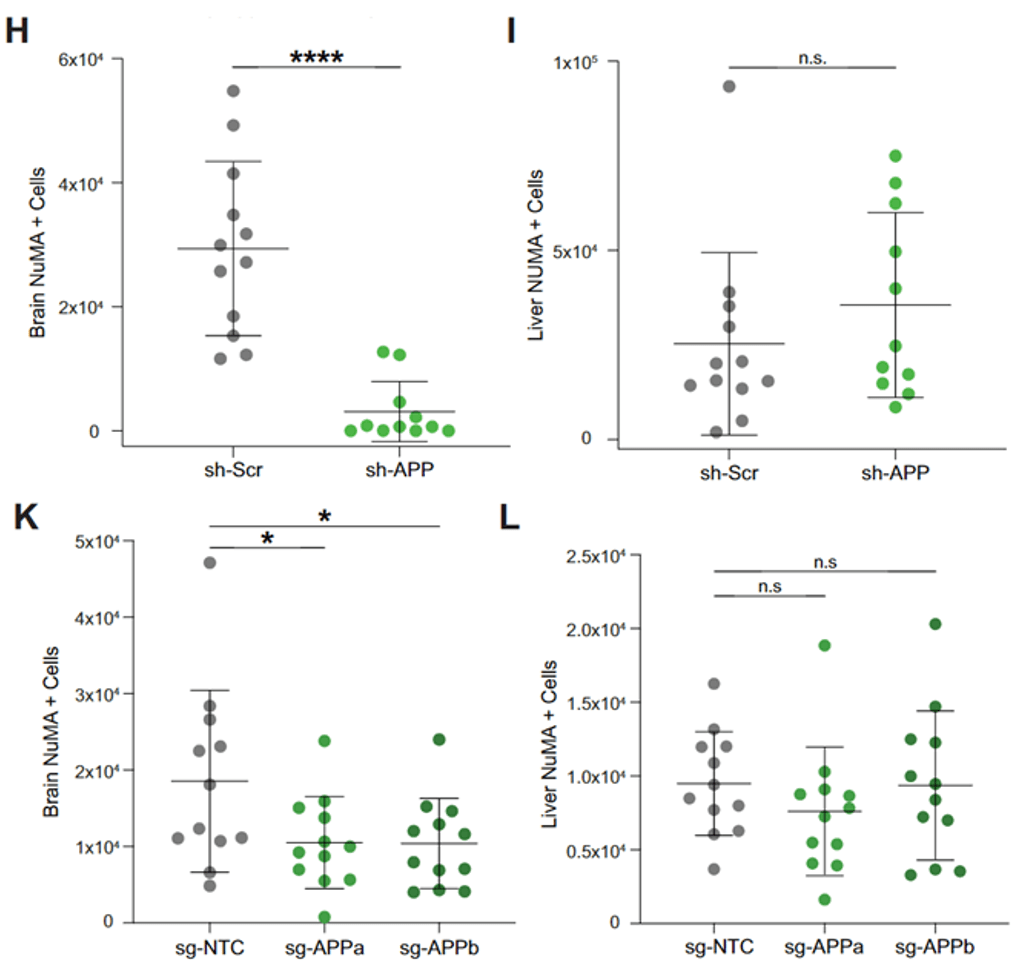
文章圖片
▲ 敲低APP后 , 腫瘤的腦轉移能力顯著下降
眾所周知 , APP是Aβ的前體 , 它擁有多種加工形式 , 所以APP發揮作用的形式到底是哪一種呢?綜合前述的研究結果 , Hernando團隊假設Aβ是APP發揮作用的形式 。
為了驗證這個猜想 , 他們進行了回補實驗 。 向已經敲除APP基因的黑色素瘤細胞中轉入突變型APP基因——SPA4CT-T43P——這種突變體基因表達產物主要是Aβ , 而不是APP的其他加工形式 。 結果顯示 ,不論是回補野生型APP基因還是突變型APP基因 , 均能夠恢復黑色素瘤細胞的腦轉移能力 。 這說明 Aβ就是黑色素瘤腦轉移所需的APP形式 。
- 綜合征|【首兒醫典】直立性蛋白尿
- 腎臟|【首兒醫典】直立性蛋白尿
- 103歲老人,40年竟沒進過醫院 沒吃一片藥,只因做了一件事!
- 視網膜|合肥普瑞眼科科普|糖尿病竟然會引發這些眼病?你一定要知道
- 兒童染幽門螺桿菌,竟然影響發育?
- 女子|廈門30歲女子肺部長腫瘤,竟是一顆痣惹的禍?醫生:要警惕
- 蛋白尿|【世界腎臟日】吾愛吾腎 知識強腎
- 腎臟|如何迅速降蛋白?醫生道出2點“秘訣”,但不少人沒意識到
- 【生活小貼士】驚!這樣剪指甲竟會導致
- 癌細胞|44歲患癌,100歲仍健在,3個習慣或讓秦怡戰勝癌細胞,分享給你
