
文章圖片
(圖源:圖蟲創意)
首批“自測版”新冠抗原檢測試劑盒來了 。
3月12日 , 國家藥監局發布通告 , 批準南京諾唯贊、北京金沃夫、深圳華大因源、廣州萬孚生物、北京華科泰生物的新冠抗原產品自測應用申請變更 。 自此五款新冠抗原自測產品正式上市 。
01
首批5家獲批
3月11日晚間 , 國家衛健委發布消息 , 經研究 , 國務院應對新型冠狀病毒肺炎疫情聯防聯控機制綜合組決定在核酸檢測基礎上 , 增加抗原檢測作為補充 , 并組織制定了《新冠病毒抗原檢測應用方案(試行)》 。
● 《方案》規定了抗原檢測的適用人群:一是到基層醫療衛生機構就診 , 伴有呼吸道、發熱等癥狀且出現癥狀5天以內的人員;二是隔離觀察人員 , 包括居家隔離觀察、密接和次密接、入境隔離觀察、封控區和管控區內的人員;三是有抗原自我檢測需求的社區居民 。 同時 , 明確了3類人群進行抗原檢測需滿足的主要條件、檢測試劑的獲得渠道 , 制定了檢測發現陽性后的處置管理流程 , 促進抗原檢測與核酸檢測相銜接 。
短短一天之后 , 五款新冠抗原自測產品正式上市 。
國家藥監局網站3月12日發布的醫療器械批準文件(變更)待領取信息顯示 , 由萬孚生物、華大基因子公司深圳華大因源醫藥科技有限公司、北京金沃夫生物工程科技有限公司、南京諾唯贊醫療科技有限公司、北京華科泰生物技術股份有限公司5家公司研發的5款新冠抗原檢測試劑盒通過了藥監局的注冊信息變更 。
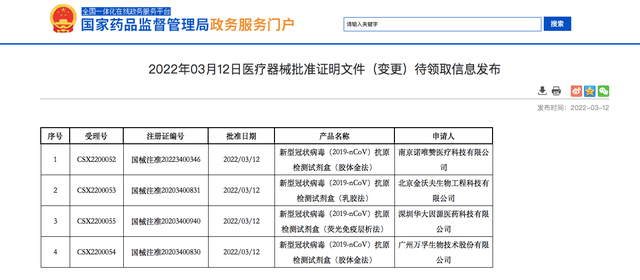
文章圖片
專業人士處獲悉 , 此次“注冊變更”的核心在于 , 不再限定該檢測試劑“僅由專業技術人員使用” 。 這意味著 , 相關檢測試劑將可用于居家自測等其他場景 。
5款新冠抗原檢測試劑盒分屬5家公司 , 其中萬孚生物、深圳華大因源(華大基因)、諾唯贊均為A股公司 , 而北京金沃夫和北京華科泰生物尚未登陸資本市場 。值得注意的是 , 北京華科泰生物2019年曾披露創業板IPO招股書 , 但最終撤回申請 。
02
擁有自測條件
事實上 , 最新獲批上市的5家公司5款新冠抗原檢測試劑盒產品 , 不少在2020年已獲批準 , 但變更注冊信息前均屬于專業版本 , 需要專業人士操作 。
具體來看 , 2020年11月 , 萬孚生物的新型冠狀病毒(2019-nCoV)抗原檢測試劑盒(膠體金法)和北京金沃夫的新型冠狀病毒(2019-nCoV)抗原檢測試劑盒(乳膠法) , 獲得國家藥監局批注上市 , 成為國內首批取得醫療器械注冊證的相關產品 。 次月 , 深圳華大因源研制的新型冠狀病毒抗原檢測試劑盒(熒光免疫層析法) , 也取得了醫療器械注冊證 。
2022年3月初 , 華科泰生物的新型冠狀病毒(2019-nCoV)抗原檢測試劑盒(熒光免疫層析法)獲批上市 , 并且很快就具備了大規模供應的產能 。
就在《方案》發布當天 , 諾唯贊醫療發布公告稱 , 全資子公司南京諾唯贊醫療科技有限公司自主研發生產的新型冠狀病毒抗原檢測試劑盒 , 近日收到國家藥監局頒發的《醫療器械注冊證》 。
諾唯贊表示 , 該試劑盒可用于檢測新型冠狀病毒感染疑似人群口咽拭子、鼻咽拭子樣本中新型冠狀病毒N抗原和S抗原 。 上述產品一般用于急性感染期 , 即疑似人群出現癥狀7天之內的樣本檢測 , 可作為核酸檢測的輔助和補充 , 配合國家新型冠狀病毒檢測策略 , 進一步提高“早發現”能力 。同時 , 公司也提醒 , 試劑盒不可單獨用于新型冠狀病毒感染的診斷 。
- 生物|國家藥監局:批準五款新冠抗原自測產品正式上市
- 江小姐|31歲女子一站立就頭疼嘔吐,原來是腦子“漏”個洞
- 疫情|壓實“四方”責任,筑牢疫情防線
- 疫情|“抗菌抗病毒”口罩靠譜嗎?國家藥監局發聲→
- 陳艷婷|3月12日0時至12時青島新增本土“15+31”
- 減肥不能碰“堅果”?建議:不想腰上長贅肉,這幾種主食需少吃
- 生物|新冠抗原自測產品正式上市
- 手術|治療精神疾病,不可“快刀斬亂麻”
- 排骨|多家醫院聯合聲明:排骨和“它”一起燉,無異于“服毒”,不少人還在吃
- 蔬菜|才知道,這5種蔬菜自帶“毒素”,吃前必須焯水,現在知道還不晚
