
文章圖片
2月10日晚間 , 國產(chǎn)PD-1腫瘤藥——信達(dá)生物(01801)信迪利單抗直面美國食品和藥物管理局(FDA)腫瘤藥物咨詢委員會(ODAC)會議審評 , 討論其基于中國臨床數(shù)據(jù)的有關(guān)聯(lián)合療法能否在美國獲批上市 。
這是國產(chǎn)PD-1腫瘤藥首次直面ODAC , 闖關(guān)FDA , 因此引發(fā)行業(yè)和投資者多方關(guān)注 。 最終ODAC要求信達(dá)生物補(bǔ)充額外的臨床試驗 , 信迪利單抗在美國上市申請暫時遇挫 。
11日信達(dá)生物發(fā)布公告稱 , 該公司將和相關(guān)方繼續(xù)與FDA配合 , 完成新藥上市申請的審評工作 。 ODAC就已上市和臨床中的腫瘤藥品 , 為FDA提供獨(dú)立的專業(yè)性意見 。 FDA在新藥審批過程中將采納ODAC的投票意見 , 但ODAC投票意見不具有對FDA決策的約束力 。

文章圖片
公告截圖
人體免疫細(xì)胞上有一個蛋白PD-1 (程序化死亡分子) , 而腫瘤細(xì)胞會產(chǎn)生一個免疫球蛋白樣的分子PD-L1(細(xì)胞程式死亡-配體1) 。 兩個分子結(jié)合時 , 會降低免疫細(xì)胞的活性 , 幫助腫瘤隱藏 。
PD-1/PD-L1抗體藥可以阻斷兩者結(jié)合 , 從而讓免疫細(xì)胞保持活性 , 殺傷腫瘤細(xì)胞 。 單抗即單克隆抗體 。 相比于化學(xué)藥物 , 單抗藥物通常不會錯誤識別和攻擊正常細(xì)胞 , 具有用藥量小、副作用小等特點(diǎn) , 多用于腫瘤治療 。
因此PD-1/PD-L1抗體藥 , 常被看作“明星腫瘤藥”、“抗癌神藥” , 備受追捧 。 以PD-1默沙東K藥為例 , 它2020年全球大賣143.8億美元 , 到2021年第三季度保持了22%的增長 。 全球范圍內(nèi)獲批的適應(yīng)癥近30種 , 甚至已有不限癌種適應(yīng)癥獲批 。
另據(jù)弗若斯特沙利文早年分析 , 到2023年 , 全球PD-1/PD-L1市場規(guī)模可以達(dá)到600億美元以上 , 中國市場也將接近千億元水平 。 綜合因素之下 , PD-1也一直被視為中國創(chuàng)新藥發(fā)展的“風(fēng)向標(biāo)” 。 恒瑞醫(yī)藥、百濟(jì)神州、君實生物和信達(dá)生物等企業(yè) , 都在該賽道上有所布局 。
官網(wǎng)信息顯示 , 信達(dá)生物成立于2011年 , 從事開發(fā)、生產(chǎn)和銷售用于治療腫瘤等重大疾病的創(chuàng)新藥物 。 2018年10月31日 , 信達(dá)生物制藥在香港聯(lián)交所主板掛牌上市 。
信迪利單抗是信達(dá)生物制藥(蘇州)有限公司自主研發(fā)的創(chuàng)新生物藥 , 由信達(dá)與禮來制藥公司共同開發(fā)和商業(yè)化 。 信迪利單抗為全人源化的IgG4單克隆抗體 , 能特異性結(jié)合T細(xì)胞表面的PD-1分子 , 阻斷這條免疫逃逸通路 , 重新激活T細(xì)胞 , 釋放細(xì)胞因子殺傷腫瘤細(xì)胞 。
信達(dá)生物方面表示 , 信迪利單抗注射液的商品名為達(dá)伯舒 。 2021年12月 , 達(dá)伯舒成為唯一一個擁有包含一線非鱗狀非小細(xì)胞肺癌、一線鱗狀非小細(xì)胞肺癌、一線肝癌及霍奇金淋巴瘤在內(nèi)的四項適應(yīng)癥獲批 , 并均被納入國家醫(yī)保的PD-1抑制劑 。
【生物|國產(chǎn)腫瘤藥首次闖關(guān)美國FDA暫時遇挫,信達(dá)生物回應(yīng)】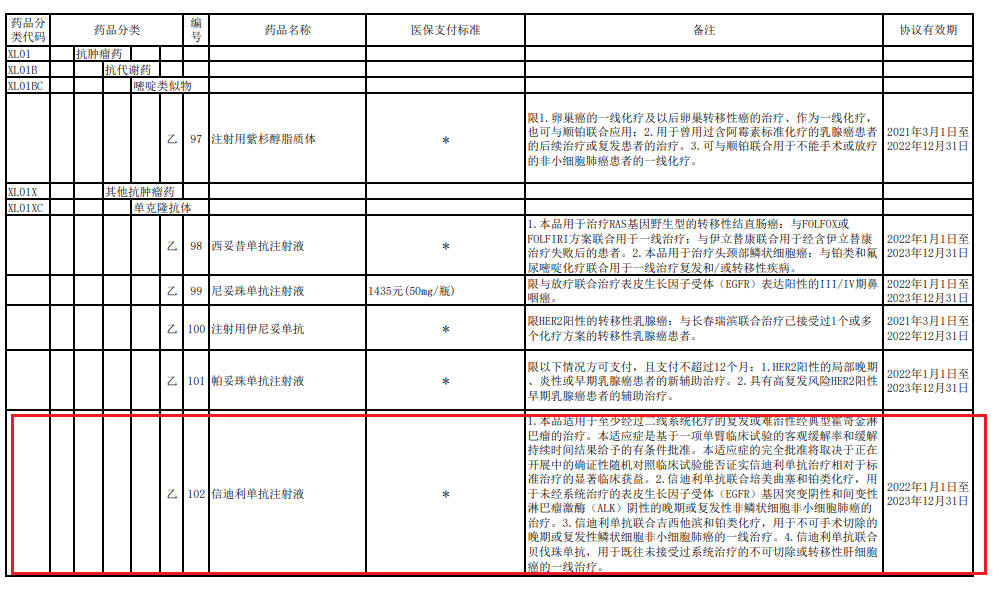
文章圖片
《國家基本醫(yī)療保險、工傷保險和生育保險藥品目錄(2021年)》 協(xié)議期內(nèi)談判藥品部分截圖
信迪利單抗此番闖關(guān)FDA暫時受阻 , 或許與其三期臨床試驗有關(guān) 。
資料顯示 , 引發(fā)中美雙方關(guān)注的ORIENT-11研究是一項評估信迪利單抗注射液或安慰劑聯(lián)合培美曲塞和鉑類用于晚期或復(fù)發(fā)性非鱗狀非小細(xì)胞肺癌一線治療有效性和安全性的隨機(jī)、雙盲、III期對照臨床研究 。
該研究共入組397例受試者 , 按照2:1隨機(jī)入組 , 分別接受信迪利單抗注射液200mg或安慰劑聯(lián)合培美曲塞和鉑類治療 , 每3周給藥1次 , 完成4個周期治療后 , 進(jìn)入信迪利單抗或安慰劑聯(lián)合培美曲塞維持階段 , 治療直至疾病進(jìn)展、毒性不可耐受或其他需要終止治療的情況 。 對照組疾病進(jìn)展后可有條件交叉至信迪利單抗單藥治療 。
- 漢娜·凱頓|花三年跨兩國,看十幾位醫(yī)生 被診斷為“壓力太大”的英國女子卵巢中取出排球大腫瘤
- 女子|花三年跨兩國,看十幾位醫(yī)生 被診斷為“壓力太大”的英國女子卵巢中取出排球大腫瘤
- 蕨菜|腫瘤主任癌癥晚期,常吃3種蔬菜,或讓你多活10年!
- 腫瘤|廈門大學(xué)附屬第一醫(yī)院:“廈”路相逢,共抗神經(jīng)內(nèi)分泌腫瘤
- 時代|狼瘡腎炎迎靶向治療時代,全球首款用于治療狼瘡腎炎的生物制劑在中國獲批
- 技術(shù)|國家藥品監(jiān)督局發(fā)布《生物類似藥臨床藥理學(xué)研究技術(shù)指導(dǎo)原則》
- 陳洪潭|27歲溫州女子沒吃兩口飯就感覺飽,食管切出巨大腫瘤狀似“麥克風(fēng)”
- 豆腐皮|“長壽老人”的秘密被發(fā)現(xiàn),我國產(chǎn)量大卻沒人吃,含鈣量比牛奶高
- 上市|要求補(bǔ)充額外臨床試驗,國產(chǎn)PD-1首次闖關(guān)FDA遇挫
- 的結(jié)果|信達(dá)生物PD-1首闖FDA受挫,被要求補(bǔ)充臨床試驗
