
文章圖片
騰盛博藥(Brii Biosciences)近期對管道中乙肝創新藥開發進展進行了更新 , 包括BRII-179(VBI-2601 , 一種在研治療性乙肝疫苗)、BRII-835(VIR-2218 , 一種在研siRNA)和BRII-877(VIR-3434 , 一種在研單抗)的多項第2期組合療法臨床開發數據 , 將在2023年全年獲得 。
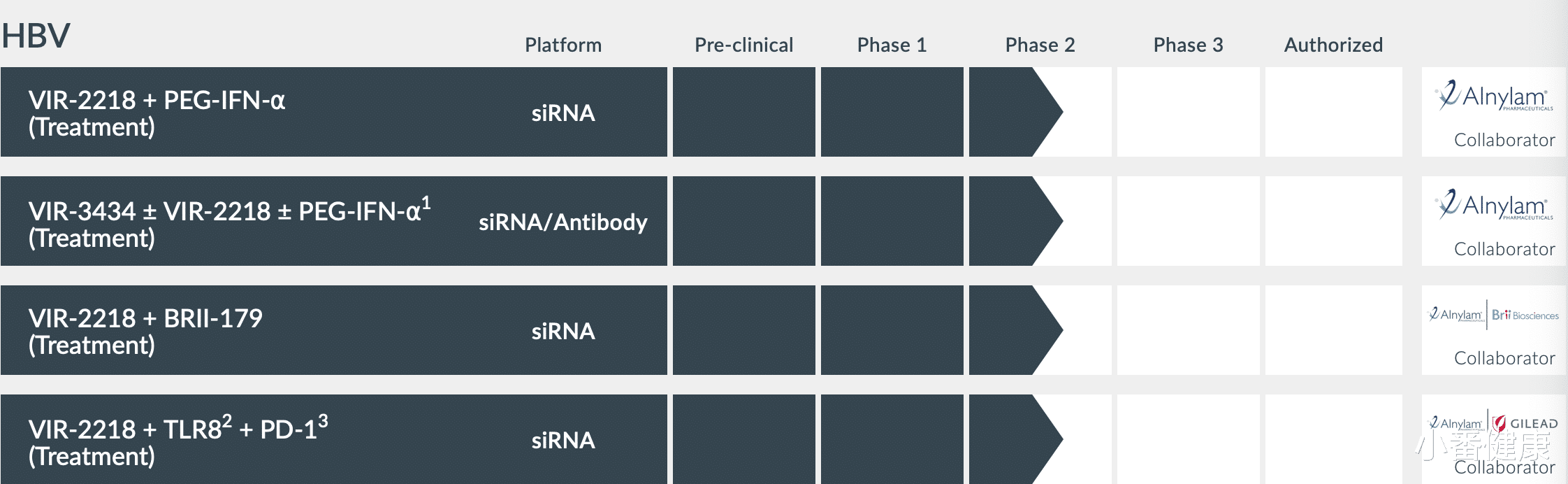
來自騰盛博藥新藥研發管道乙肝制藥更新 , 由VIR進行兩項2期組合 , 將在今年上半年獲得數據
研發特點和作用機理方面 , 騰盛博藥介紹 , BRII-179是一種基于重組蛋白的新型HBV免疫療法候選藥物 , 表達Pre-S1、Pre-S2和S HBV表面抗原 , 旨在誘導增強B細胞和T細胞免疫 。 BRII-835是一種GalNAc結合的小干擾核糖核酸(siRNA) , 其靶向所有的HBVRNA , 已證明可阻斷病毒轉錄步驟 , 減少病毒蛋白并減輕免疫抑制 。
BRII-877是一種研究階段皮下注射HBV中和單抗 , 旨在阻斷所有10種基因型的HBV進入肝細胞 , 同時降低血液中病毒和亞病毒顆粒的水平 。 BRII-877結合了Xencor公司的Xtend?和其他Fc技術 , 被設計成有可能作為T細胞疫苗來對抗感染病人的HBV , 并具有延長的半衰期 。
來自VBI Vaccines新藥管道目前 , 騰盛博藥正與Vir Biotechnology公司、VBI Vaccines公司合作開發上述乙肝創新機制候選藥物 。 2022年至2023年已完成及將要到來的上述候選藥物臨床開發進度如下:
由騰盛博藥進行的BRII-179(VBI-2601)+BRII-835(VIR-2218)2期組合療法:2023年2月 , 在亞太肝臟年會上(APASL2023)已公布該試驗中期數據 , 結果表明該組合療法具有良好的安全性和耐受性 , 相較于單用BRII-835(VIR-2218)或BRII-179(VBI-2601) , 該組合療法可誘導更強抗乙肝表面抗原(HBsAg)抗體反應 , 并導致改善HBsAg特異性T細胞反應 。
本屆亞肝會公布數據顯示 , 所有隊列中的50名受試者在治療結束時實現了乙肝表面抗原水平下降 , 平均降幅為 -1.7至-1.8 log 10 IU/ml 。 有2名受試者 , 在第40周時實現了乙肝表面抗原水平的最大降幅 , 達到或低于定量下限(LLOQ) , 同時還有強大的HBsAg特異性抗體和T細胞反應 。 該2期組合療法其他數據 , 預計將在今年下半年公布!
由騰盛博藥進行的BRII-179(VBI-2601)+ PEG-IFN-α另一項2期組合療法:2022年12月 , 騰盛博藥已完成該2期試驗第一部分的受試者招募工作 , 評估在已接受PEG-IFN-α和NRTI治療的慢性HBV受試者中加入BRII-179(VBI-2601 , 一種在研治療性乙肝疫苗) 。 該2期組合療法預計將在今年下半年獲得頂線結果 。
由Vir Biotechnology公司進行的VIR-2218(BRII-835)+ PEG-IFN-α第2期組合療法:在去年美肝會上 , VIR公司已經介紹了這項正在進行的2期組合療法48周治療結束數據 , 數據顯示 , 近31%的慢性HBV受試者 , 實現了HBsAg血清清除與抗HBs血清轉換 , 且無新的安全信號!該2期組合療法其他數據 , 預計將在今年上半年公布 。
由Vir Biotechnology公司進行的VIR-2218(BRII-835)+VIR-3434(BRII-877)第2期組合療法MARCH試驗:VIR公司已在去年美肝會上介紹了這項正在進行的MARCH第2期研究的A部分初始治療結束數據 , 該試驗是指在接受NRTI療法的慢性HBV感染受試者中使用VIR-2218(BRII-835)+VIR-3434(BRII-877)組合療法!
結果表明 , 即以小干擾RNA+皮下注射HBV中和單抗的組合療法對乙肝表面抗原水平的減少量是相輔相成的 , 在所有受試者中 , 對乙肝表面抗原的減少量方向 , 該組合療法均遠大于單一療法 , 且無安全信號 。 正進行該2期MARCH試驗A部分的其他數據 , 預計將在今年上半年公布 。
- 河豚|乙肝制藥更新,APG-1387小分子IAP抑制劑,截至2023年初開發進展
- |老撾第二制藥廠恩曲替尼(Entrectinib)PHOENTRE說明書
- 便秘|乙肝在研新藥HB-400,吉利德科學牽頭,2023年將進入1期首例用藥
- 疾病|乙肝制藥更新,VBI-2601兩項正進行II期研究,整個2023年發布數據
- 乙肝|乙肝/丁肝在研新藥REP 2139,通過SC,挽救BLV失敗及反彈數據
- 乙肝|乙肝在研新藥ALG-000184,無論HBeAg狀態,迅速降低HBVDNA及HBsAg
- 乙肝|乙肝在研新藥HepTcell,2期入組率完成90%,2024年上半年讀出數據
- 肝功能檢查,能查出乙肝小三陽嗎?有乙肝,擔心入職體檢不合格
- 抽煙不但傷肺、傷血管,也大大增加乙肝患者肝癌發病率
- 慢性乙肝病毒不過是紙老虎而已,堅信一句話:自助者天助!
