
文章圖片
文章圖片

非酒精性脂肪性肝炎(NASH)是一種除酒精外由其他各種因素導致的肝細胞內脂肪堆積和肝小葉內炎癥為特征的臨床病理綜合征 , 由非酒精性脂肪肝病(NAFLD)進展而來 , 并可發展成肝硬化甚至肝癌 。
圖源網絡 , 如有侵權請聯系作者刪除
目前全球已經有超過1億非酒精性脂肪性肝炎患者 , 他們的肝硬化和肝癌風險顯著升高 。 據最新數據顯示 , 非酒精性脂肪性肝炎(NASH)已成為我國慢性肝病的主要病因之一 , 嚴重影響著公眾的健康 。
治療非酒精性脂肪肝炎(NASH)的藥物研發難度大 , 進展緩慢 , 一直被視為研發行業的黑洞 。 近年來 , 雖然針對非酒精性脂肪肝炎(NASH)的靶向藥物研究取得了積極進展 , 但是 , 該病尚無獲批的針對性療法 。 今年 , 非酒精性脂肪肝炎(NASH)患者們終于看到了希望 。
據2023年9月13日消息 , 美國FDA已受理瑞司美替羅(resmetirom)治療伴有肝纖維化的非酒精性脂肪性肝炎(NASH)成年患者的新藥申請(NDA) , 并授予其優先審評資格 , 美國FDA完成新藥上市申請審批的截止日期為2024年3月14日 。
據悉 , 瑞司美替羅的上市申請于2023年7月中旬向美國FDA提交 , 用于治療伴肝纖維化的非酒精性脂肪性肝炎(NASH)成人患者 。 此時 , 距離上市申請的提交僅僅過去兩個月時間 。
瑞司美替羅是一種每日一次的口服甲狀腺激素受體(THR)-β選擇性激動劑 。 在關鍵性3期MAESTRO-NASH系列試驗中 , 瑞司美替羅同時實現了肝組織學改善終點——非酒精性脂肪性肝炎的消退和肝纖維化的減輕 。
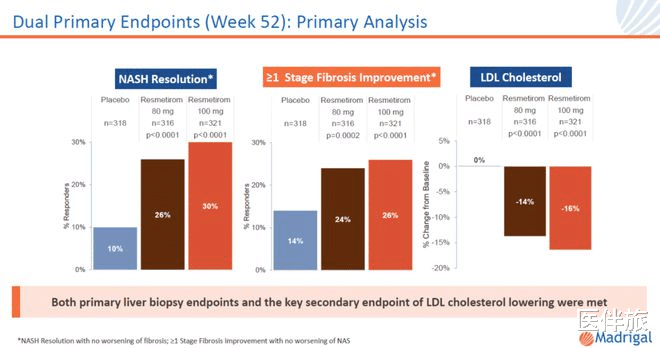
研究結果顯示 , 兩個給藥組達到52周主要終點非酒精性脂肪性肝炎消減的比例分別為26%及30% , 安慰劑組為10%;兩個給藥組達到52周主要終點纖維化改善的比例分別為24%及26% , 安慰劑組為14% 。 (見圖一)
圖一
此外 , 瑞司美替羅還達到試驗的多項次要終點 , 顯著降低多種脂質、脂蛋白、低密度脂蛋白膽固醇(LDL-C)指標 。 在關鍵次要終點上 , 80 mg給藥組在24周的低密度脂蛋白膽固醇(LDL-C)平均改變為 -12% , 100 mg組為 -16% , 而安慰組的改變為平均1% 。 (見圖二)
【肝脂肪降低51%!瑞司美替羅上市申請獲FDA優先審評資格】圖二
利用基于核磁共振的無創檢測手段對肝臟脂肪水平的評估顯示 , 接受瑞司美替羅100 mg治療52周后 , 患者肝臟脂肪水平平均降低51% 。 肝纖維化、肝臟體積和脾臟體積也顯著降低 。 (見圖三)
圖三
安全性方面 , 與安慰劑組相比 , 瑞司美替羅組報告的最常見不良事件(頻率更高)是治療開始時出現的一般輕微且短暫的腹瀉和惡心 。
參考資料:
1.Madrigal Pharmaceuticals Announces NDA Acceptance and Priority Review of the New Drug Application for Resmetirom for the Treatment of NASH with Liver Fibrosis. Retrieved September 13 2023 from
https://ir.madrigalpharma.com/news-releases/news-release-details/madrigal-pharmaceuticals-announces-nda-acceptance-and-priority.
2.Madrigal Announces Positive Topline Results from the Pivotal Phase 3 MAESTRO-NASH Clinical Trial of Resmetirom for the Treatment of NASH and Liver Fibrosis. Retrieved September 13 2023 from https://ir.madrigalpharma.com/news-releases/news-release-details/madrigal-announces-positive-topline-results-pivotal-phase-3.
- 肝病別拖延,若是上廁所出現這3種現象,或許是肝受損了
- 帕梅拉火爆Youtube徒手訓練,堪稱脂肪殺手
- JAMA:斑塊縮小1%,就可顯著降低心血管風險!做好3點,或可“逆轉”斑塊
- 胸膜炎、肝腹水、腎性水腫,一個“千古”良方,4味中藥保駕護航
- 4個減脂餐原則,降低熱量攝入,讓你不知不覺瘦下來
- 經常放屁就是肝不好?出現2個癥狀需警惕,或是疾病預兆
- 肝變硬,頭先知?醫生提醒:頭部若出現這3種情況,建議重視起來
- 研究速遞:老年人每天走夠這些步,降低近一半心腦血管風險!
- WHO發布新指南:脂肪、碳水化合物怎么吃更健康?
- 多吃素也可能得脂肪肝?脂肪不是最大威脅,揭示4大被忽略的元兇
